Os filtros respiratórios constituem uma barreira eficaz que evita a contaminação cruzada entre os doentes, os sistemas respiratórios, o equipamento respiratório e anestésico e o ambiente clínico. A sua utilização é amplamente reconhecida como benéfica e é recomendada por várias associações de anestesistas1. São amplamente utilizados em todo o hospital, particularmente no bloco operatório, nos cuidados intensivos, nas unidades de função pulmonar e nas unidades de cuidados respiratórios.
Os permutadores de calor e humidade (HME) minimizam as perdas de gases expirados pelos doentes. Quando combinados com um filtro (filtro permutador de calor e humidade, HMEF), também reduzem o risco de contaminação cruzada no ambiente clínico.
Páginas relacionadas
- Filtragem e humidificação
- Filtros respiratórios
- HMEs e HMEFs
- Filtros para aparelhos respiratórios
- Glossário
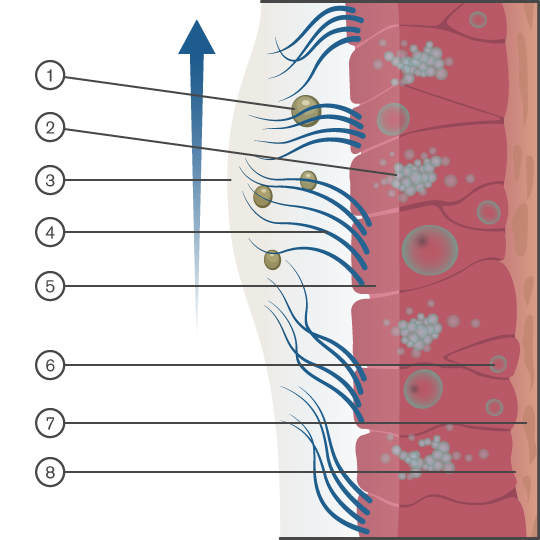
Deslocação do muco para a faringe
A função normal das vias respiratórias superiores do corpo é filtrar, humidificar e aquecer o ar que respiramos. O ar é aquecido ao passar por uma vasta rede de capilares no nariz. As membranas mucosas revestem as vias respiratórias superiores e ajudam a humedecer o ar e a reter as partículas transportadas pelo ar (poeiras e micróbios). Os cílios deslocam o muco para longe dos pulmões e em direção à faringe para ser removido.
As vias respiratórias superiores também ajudam a conservar o calor e a humidade que, de outra forma, se perderiam durante a respiração normal. O gás que sai dos pulmões durante a expiração estará à temperatura do corpo (37°C) e terá uma Humidade Absoluta (AH) de 44mg/l H2O e uma Humidade Relativa (RH) de 100%. À medida que o doente expira, o calor e a humidade são retidos pelas vias aéreas superiores e depois transferidos para o gás inspirado, que é normalmente mais frio e seco, dependendo das condições ambientais. A grande área de superfície das vias respiratórias superiores torna-a particularmente eficiente. Isto ajuda a minimizar quaisquer potenciais efeitos secundários associados à respiração de gases frios e secos durante um período prolongado.
Esta proteção fisiológica natural é contornada quando é inserido um dispositivo de via aérea artificial, por exemplo, um tubo traqueal, uma via aérea supraglótica ou um tubo de traqueostomia. Isto significa que a fonte de gás tem uma via direta para os pulmões delicados e sensíveis, o que pode resultar num aumento do risco de infeção e de potencial contaminação cruzada microbiana.
Pode também resultar num arrefecimento e secagem das vias respiratórias em resultado da respiração de gases medicinais frios e secos durante um período de tempo prolongado. O ar ambiente estaria normalmente a cerca de 23°C, com uma HR de 60% e um AH de 21mg/l. Os gases medicinais estariam normalmente a 10-15°C, com uma HR de 0-2% e um AH de 0,5 mg/l, o que aumentaria ainda mais o risco. Isto pode provocar danos nos cílios, muco mais espesso e crostas de muco, o que aumenta o risco de oclusão do tubo, o risco de infeção, atelectasia e custos acrescidos devido ao prolongamento do internamento hospitalar.
Chave de diagrama: 1. Partículas. 2. Célula mucosa 3. Camada de muco 4. Cílios 5. Chamada epitelial colunar ciliada. 6. Célula estaminal 7. Lamina propria 8. Membrana basal
Ambiente clínico
Infeção
Proteger o doente
Os doentes em estado crítico com imunidade reduzida correm normalmente um risco acrescido de infecções. Estas infecções nosocomiais resultam numa maior morbilidade e potencial mortalidade, além de terem um impacto significativo no custo do tratamento do doente devido ao aumento do tempo de internamento. A utilização estratégica de um filtro respiratório eficiente e devidamente validado proporciona uma barreira eficaz entre o doente, os sistemas respiratórios e o equipamento respiratório, o que reduz o risco de contaminação cruzada.
Contaminação cruzada
Proteção do sistema respiratório
Os doentes que necessitam de uma via aérea artificial têm a sua proteção fisiológica natural contornada. Isto aumentará o risco de infeção e de contaminação cruzada entre os doentes e o equipamento de cuidados de saúde. A contaminação cruzada de doentes através de um sistema anestésico foi registada e documentada(2). As áreas de preocupação relativamente à infeção incluem a hepatite C, o Mycobacterium tuberculosis, o sangue na expetoração, a SRA e os coronavírus semelhantes.
Proteção do equipamento respiratório e do ambiente clínico
Proteção do equipamento
A utilização de filtros respiratórios adequados e eficazes pode proporcionar proteção a equipamento delicado e dispendioso, ajudando a preservar a funcionalidade, a reduzir os custos de funcionamento e a reduzir a potencial contaminação cruzada.
Eficiência comprovada
Cada vez mais, a única forma de um médico poder determinar a eficiência e a eficácia do desempenho de um filtro respiratório, HME e HMEF é através de protocolos de teste e resultados normalizados. É vital garantir que os dados são clinicamente relevantes, actualizados e reflectem o produto que o cliente está a utilizar.
A nossa gama de filtros respiratórios e HMEFs foi testada de forma independente e provou ser altamente eficiente na prevenção da passagem de bactérias e vírus. Estes testes fornecem informações clinicamente relevantes para permitir a tomada de decisões baseadas em provas sobre o produto mais adequado para satisfazer os seus requisitos clínicos.
Testes microbiológicos
Todos os nossos filtros são testados em laboratórios especializados em microbiologia contra desafios bacterianos e virais clinicamente relevantes. Isto é normalmente efectuado numa instalação de testes independente que desenvolve protocolos específicos para simular os tipos de desafios que um filtro pode enfrentar no contexto clínico.
É escolhida uma partícula de desafio para simular o tamanho das bactérias e vírus que ocorrem habitualmente. Cada filtro Intersurgical e HMEF individual é testado e o seu desempenho é verificado desta forma.
São efectuados testes clinicamente relevantes em todos os produtos utilizando Bacillus subtilis (1,0µm x 0,7µm) e bacteriófago Ø174 (0,027µm).
Vírus potencialmente infecciosos [Tamanhos das partículas μ microns]

1. Colifago T1 [0.017μ]
2. MS-2 colifago [0.02μ]
3. Hepatite C [0.03μ]
4. Adenovirus [0.07μ]
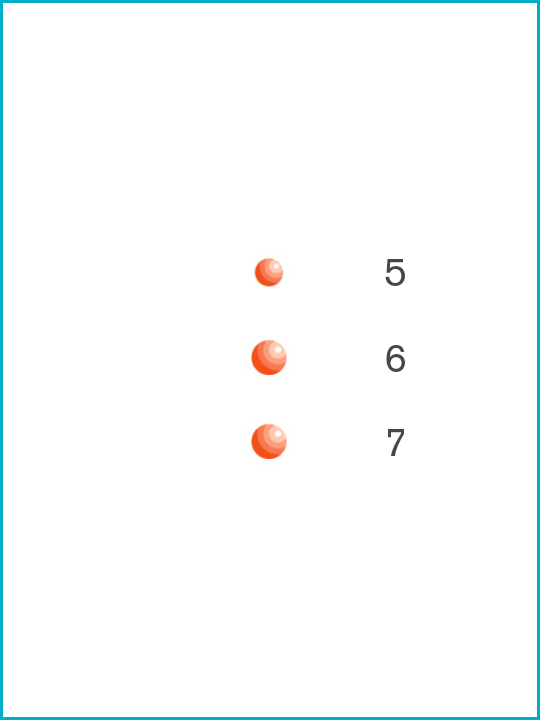
5. VIH [0.11μ]
6. Orthomyxovirus [0.1μ]
7. Cytomegalovirus (CMV) [0.1μ]
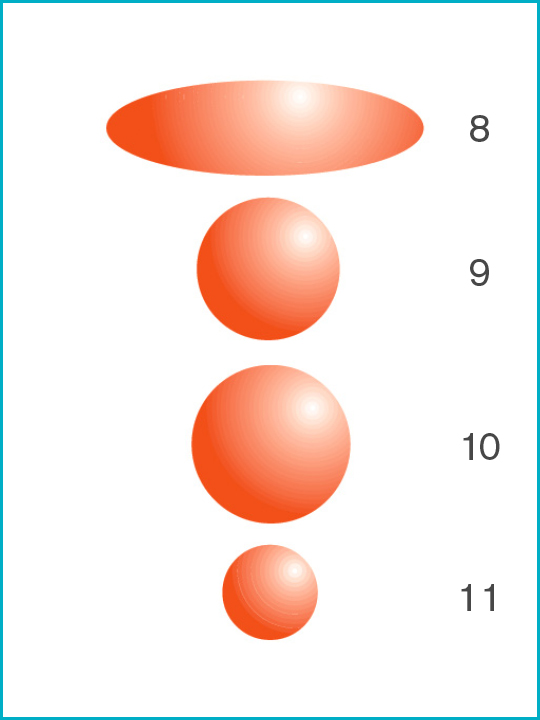
8. Mycobacterium tuberculosis [0.3μ x 1.0μ smallest size]
9. Serratia marcescens [0.45μ]
10. Pseudomonas aeruginosa [0.5μ]
11. Brevundimonas diminuta [0.3μ]
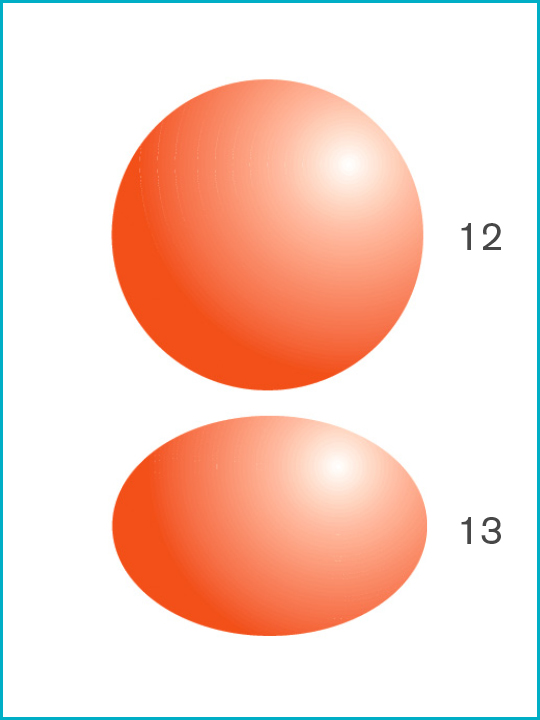
12. Staphylococcus aureus [1.0μ]
13. Bacillus subtilis [1.0μ x 0.7μ]
O nível de avanço do desafio determina a eficiência. Esta eficiência é comunicada como uma percentagem baseada neste avanço quando comparado com o desafio.
| Número de organismos que desafiam o filtro | Número de organismos que passam pelo filtro | Eficiência do filtro |
| 100,000 | 1000 | 99% |
| 100 | 99.9% | |
| 10 | 99.99% | |
| 1 | 99.999% |
O desafio apresentado no protocolo de teste viral (bacteriófago φ174, 0,027 μm) será pelo menos tão grave como o colocado pelo Coronavírus (COVID-19). As declarações de desempenho estão disponíveis mediante pedido para produtos individuais.
O surto de COVID-19 afectou a maioria dos países e, infelizmente, causou milhares de mortes em todo o mundo.
A gama de filtros respiratórios intra-cirúrgicos e HEMF foi testada independentemente e provou ser altamente eficiente na prevenção da passagem de bactérias e vírus no ambiente de cuidados de saúde.

Todos os produtos que possuem um filtro foram testados de acordo com os requisitos da norma ISO 23328-2003 e estão em conformidade com os mesmos.

Com base no tamanho e na forma do coronavírus da COVID-19 (0,05-0,1 mícron) e nos dados de testes virais mais rigorosos em arquivo, que utilizam uma partícula de desafio de 0,027 mícron, pode confirmar-se que a gama Intersurgical proporcionará, pelo menos, o mesmo nível de proteção contra a COVID-19 que o relatado nos testes microbiológicos independentes. Cópias disponíveis mediante pedido.
Código de cores para facilitar a seleção
A nossa gama de filtros respiratórios, permutadores de calor e humidade (HMEs) e filtros permutadores de calor e humidade (HMEFs) está codificada por cores para facilitar a identificação e para garantir que é utilizado o filtro/HME correto, minimizando qualquer risco potencial para o doente.
Referência 1: Association of Anaesthetists of Great Britain and Ireland 1996. Sociedade Dinamarquesa de Anestesistas 1998. Sociedade Francesa de Anestesistas 1998
Referência 2: Chant K, Kociuba K, Munro R, et al. Investigation of possible patient-to-patient transmission of hepatitis C in a hospital. NSW Public Health Bull 1994; 5:47-51.